03 · 常见实验
TIP
部分实验在前文已经提及,此处不再赘述。
物质制备类 (气体、无机物、有机物):掌握试剂选择、反应原理、装置搭建、除杂干燥
分离提纯类(过滤、蒸发、蒸馏、萃取、分液、洗涤、干燥):掌握操作要点、仪器选择、适用范围
定量测定类(滴定、量气、称重):掌握误差分析、计算方法、操作规范
性质探究类(氧化还原、速率、平衡):掌握控制变量、现象分析、原理推导
离子检验 & 物质推断:掌握试剂选择、现象判断、排除干扰
粗盐提纯
实验:溶解 → 过滤 → 蒸发 → 除杂(
试剂及作用:
溶液:除去粗盐中的 溶液:除去 和过量的 溶液:除去 - 稀
:除去过量的 和
反应方程式:
; ;
知识点:
- 过滤操作需遵循“一贴、二低、三靠”的原则
- 除杂顺序:
→ → → - 蒸发:当出现大量固体时停止加热,利用余热蒸干剩余液体
注意事项:除杂时
蒸馏 & 萃取分液
(1)蒸馏(物理变化)
考点:适用对象、装置、操作 试剂及作用:碎瓷片/沸石:防止液体暴沸 知识点:
- 蒸馏适用于沸点不同的物质分离
- 温度计水银球需放在支管口处
- 冷凝水需“下进上出”,加入碎瓷片可防止暴沸 题型:装置图判断、选择、操作改错 注意事项:蒸馏时温度计水银球不能插入液面下;冷凝水“下进上出”保证冷凝充分;蒸馏烧瓶需垫石棉网加热。
(2)萃取分液(物理变化)
考点:适用对象、萃取剂选择、分液操作 试剂及作用:
- 可用
萃取溴水或碘水中的 、 - 分液操作时需先放出下层液体,再倒出上层液体 题型:装置图判断、选择、操作改错 注意事项:萃取剂不能与原溶剂互溶(如不能用酒精萃取碘水);分液时下层液体从下口放出,上层液体从上口倒出,避免交叉污染;振荡分液漏斗后需放气。
一定物质的量浓度溶液配制
知识点:
- 配制步骤:计算 → 称量 → 溶解 → 冷却 → 转移 → 洗涤 → 定容 → 摇匀
- 所需仪器:容量瓶、烧杯、玻璃棒、胶头滴管、托盘天平/量筒
- 误差判断:俯视读数偏小,仰视读数偏大 注意事项:溶解后的溶液需冷却至室温再转移至容量瓶(防温度过高影响容量瓶精度);洗涤烧杯和玻璃棒
次,洗涤液全部转移至容量瓶;定容时胶头滴管垂直悬空,不接触容量瓶内壁。
制备
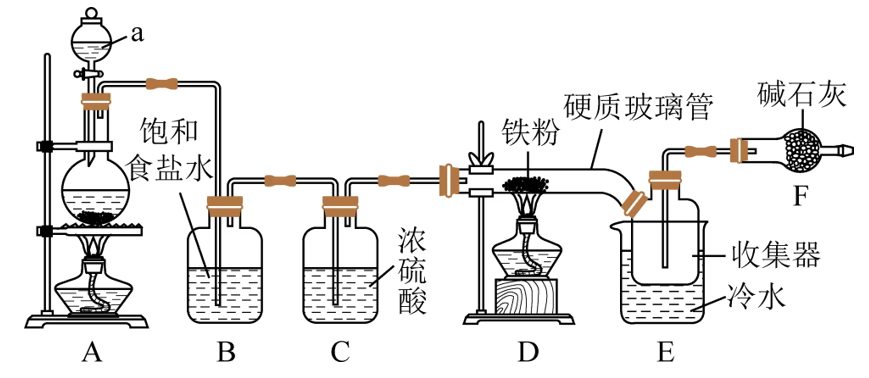
- A:
- B(饱和食盐水):吸收氯化氢气体
- C(浓硫酸):除去氯气中的水分
- E:
易升华,使用冷水使其变为固体,方便收集 - F(碱石灰):Ⅰ尾气吸收;Ⅱ防止外界水蒸气进入
水解程度较大( ),因此要注意不能使外界水蒸气进入,同时如果要制备 溶液时,应先将 固体溶于少量盐酸(使反应逆向移动),再加水稀释。
化学平衡移动(以
试剂及作用:
溶液、 溶液:建立 平衡 - 浓
/ 溶液:改变离子浓度 球:建立 平衡,热水/冷水改变温度
反应方程式:
(血红色) (红棕色) (无色)
注意事项:
- 探究单一变量时,需保证其他条件相同(如探究温度影响时,浓度、催化剂用量一致)
- 催化剂只改变反应速率,不影响平衡移动
- 观察现象时需及时记录,避免因反应放热/吸热导致温度变化干扰实验
弱电解质电离 & 盐类水解
(1)弱电解质的电离(盐酸/醋酸对比)
实验:同浓度盐酸/醋酸 pH、导电性 反应方程式:
(2)盐类的水解
试剂及作用:
、 、 溶液:不同类型盐,测酸碱性 - pH 试纸:判断溶液酸碱性
- 酚酞/石蕊:显色剂
反应方程式:
(或写作 )
知识点:
- 弱电解质电离不完全,强电解质电离完全
- 盐类水解规律:越弱越水解,谁强显谁性
注意事项:
- 测 pH 时,pH 试纸需干燥,不能湿润(避免稀释溶液影响结果)
- 导电性实验需在相同温度下进行(温度影响离子迁移速率)
- 盐类水解吸热,加热可促进水解,需控制实验温度一致
沉淀溶解平衡
实验:沉淀转化(
溶液:提供 ,生成 沉淀 溶液:提供 溶液:提供 ,实现 → 转化 溶液:提供 ,实现 → 转化
反应方程式:
注意事项:
- 沉淀转化实验需控制离子浓度一致,确保实验现象由
大小决定 溶液需少量滴加,避免过量导致现象干扰 - 实验后废液需处理(含重金属离子),不能直接排放
电化学(原电池 & 电解池)
(1)原电池(以铜锌原电池为例)
试剂及作用:
片、 片:电极( 为负极, 为正极) - 稀
/ / 溶液:电解质溶液,提供离子,形成闭合回路
反应方程式:
- 负极(
): (氧化反应) - 正极(
): - 酸性电解质:
- 硫酸铜电解质:
- 酸性电解质:
- 总反应:
(2)电解池(以电解饱和食盐水、电解
试剂及作用:
- 石墨电极/
电极:阳极/阴极 - 饱和
溶液/ 溶液:电解质溶液 - 淀粉-
试纸:检验电解食盐水生成的
反应方程式:
- 电解
(石墨电极): - 阳极:
- 阴极:
- 总反应:
- 阳极:
- 电解饱和食盐水(石墨电极):
- 阳极:
- 阴极:
- 总反应:
- 阳极:
知识点:
- 原电池:负极发生氧化反应,正极发生还原反应(负氧正还)
- 电解池:阳极发生氧化反应,阴极发生还原反应(阳氧阴还)
注意事项:
- 原电池两极需为不同活泼性金属(或一极为非金属导体),电解质溶液需能与负极反应
- 电解池阳极若为活性电极,电极本身参与反应