04 · 原电池 整理中
原电池基本概念
日常电能大多数来自火力发电,化学能通过能量转化,间接转化为电能。
过程如下:
化学能
缺点: 步骤多、效率低、环境污染
原电池——化学能直接转化为电能
实验过程:
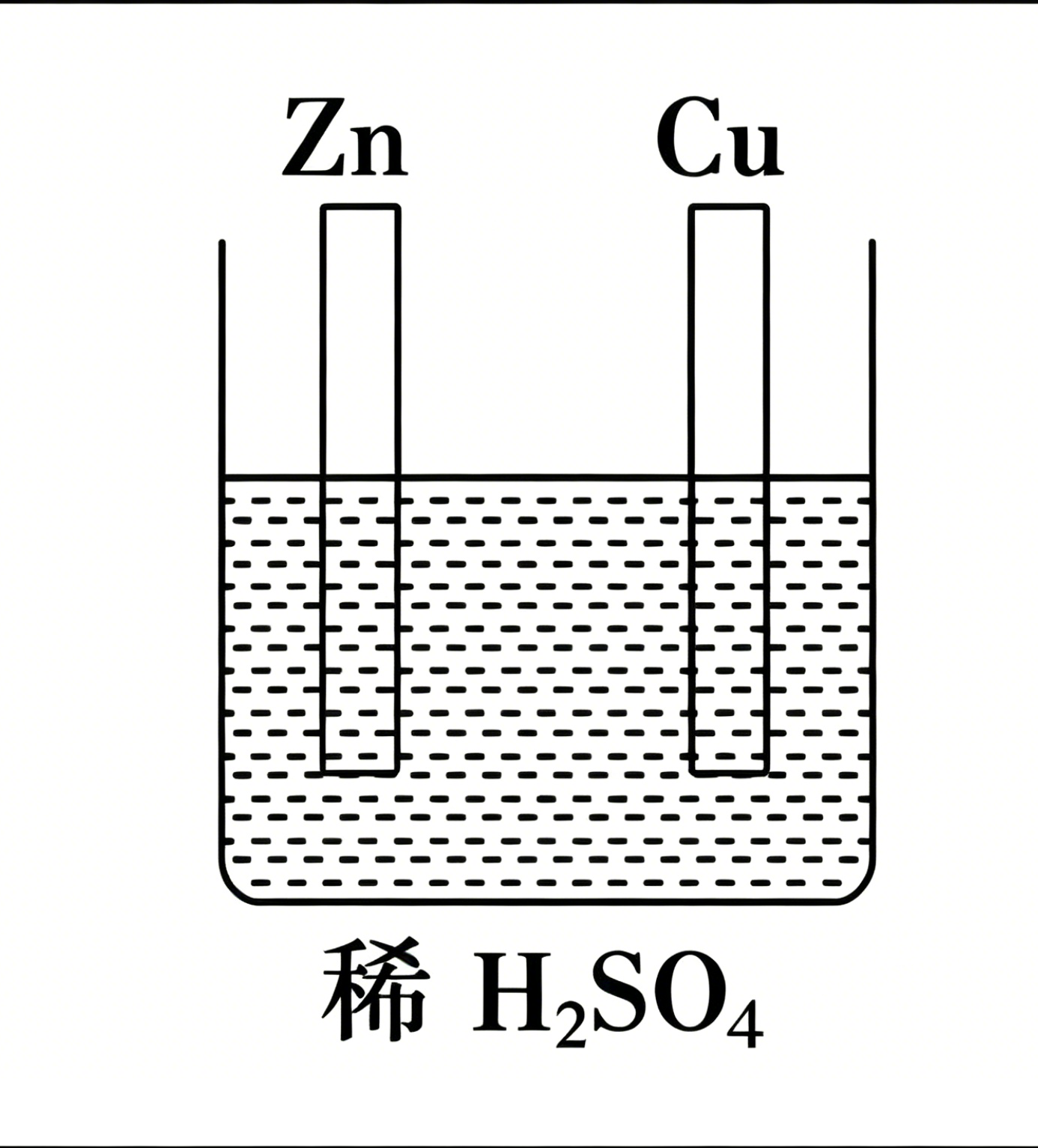 | 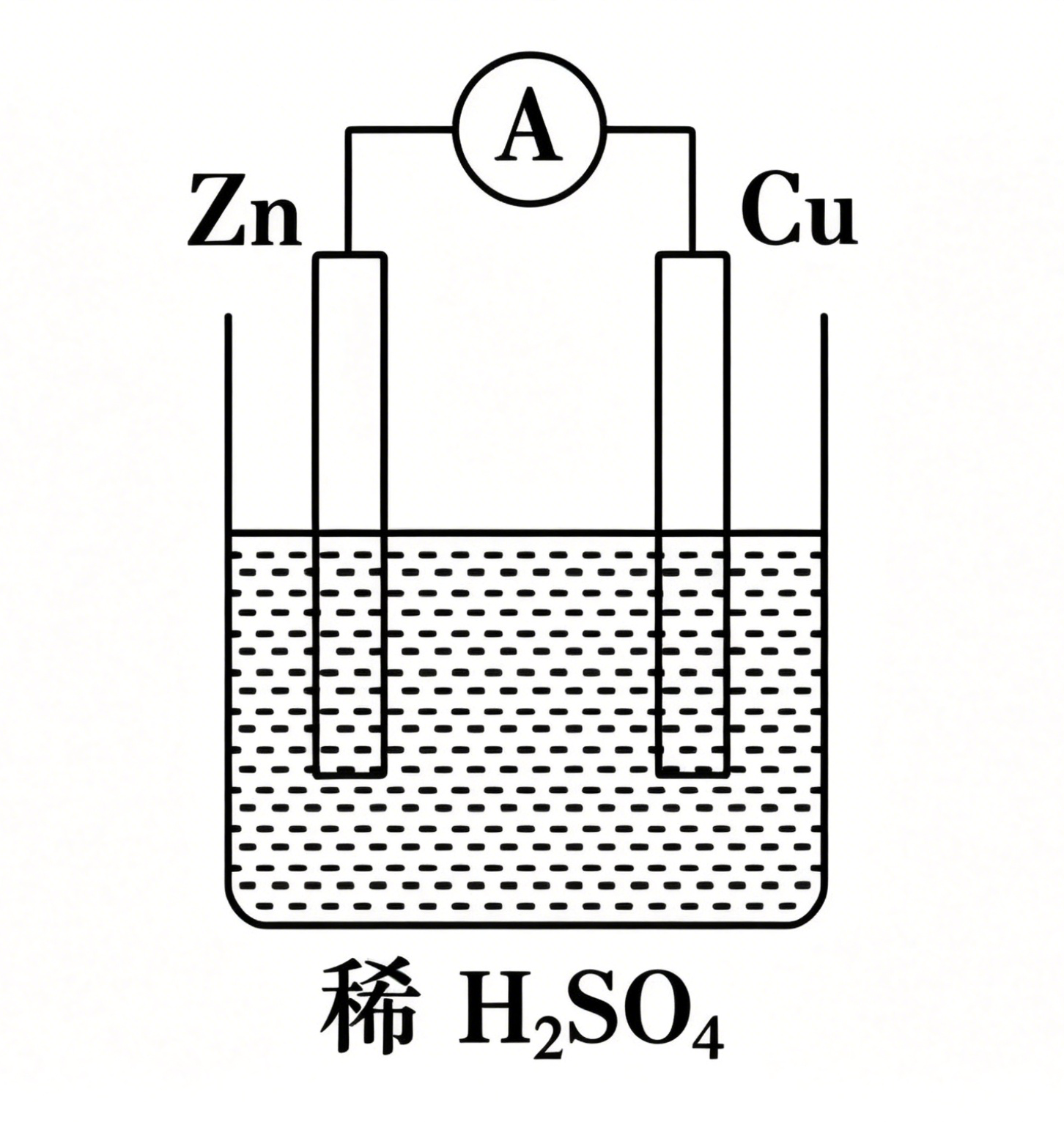 |
|---|---|
| 锌和 | 锌片逐渐溶解 (锌的电子通过电线接触铜从而和稀硫酸反应) |
| 铜片无反应 | 铜片上有气泡产生 (铜只导电,不和稀硫酸反应) |
| 无电流产生 | 导线中有电流通过 |
定义: 利用氧化还原反应原理,将化学能转化为电能的装置
负极失去电子经外电路流入正极的过程中形成电子流,被人类利用
电子流:负极
电流:正极
构成条件
理论上,自发的氧化还原反应均可构成原电池。
- 有活动性不同的两个电极
- 溶液:两电极均插入电解质溶液中
- 导线:两电极用导线相连,形成闭合回路
化学电池
概念: 化学电池是根据原电池原理,将化学能转变为电能的装置。
分类: 可分为一次电池,二次电池和燃料电池。
- 一次电池:
放电后不能再充电使其复原的电池(内部氧化还原反应无法逆向进行)。 - 二次电池:
又称为充电电池或蓄电池,放电后可以再充电,可以多次重复使用。 - 燃料电池:
利用燃料和氧化剂之间发生氧化还原反应,能连续地将燃料和氧化剂的化学能直接转化为电能的化学电池,如氢氧燃料电池,甲醇燃料电池。
设计原电池
盐桥
- 组成: 固定剂是琼脂,电解质溶液常见的有饱和
溶液或饱和 溶液。 - 作用: 连接内电路,形成闭合回路,使溶液电荷守恒,便于源源不断产生电流,避免氧化剂,还原剂直接接触,增大化学能,转化成电能的效率。
- 离子移动的方向: 阳离子往正极移动,阴离子往负极移动。